Sysmex si tinge di rosa – Contrastiamo insieme il cancro mammario!
Il cancro mammario è il tipo di patologia maligna più frequentemente diagnosticato nelle donne [1]. Pur tuttavia, una precoce individuazione attraverso regolari esami di screening e genetici per evidenziare una predisposizione può incrementare le probabilità di cura di questa malattia e renderla, in molti casi, evitabile.
L’applicazione di nuovi strumenti diagnostici molecolari combinati con approcci chirurgici meno invasivi e trattamenti personalizzati ha, inoltre, migliorato significativamente l’esito dal punto di vista oncologico e la qualità di vita del paziente.
In questi miglioramenti, il ruolo che a noi spetta è importante, dal momento che offriamo un’ampia gamma di prodotti innovativi che ricoprono l’intero processo di gestione di un cancro mammario.
Metodi di prevenzione del cancro mammario
In molti casi, il cancro mammario su base ereditaria è dovuto alla presenza di una mutazione (ereditaria) deleteria a livello della linea germinale nei geni BRCA1 e/o BRCA2 [2].
Prima di essere sottoposto ad esami, un soggetto verrà di norma valutato dal punto di vista del rischio, laddove questa valutazione avviene attraverso l’incontro con un consulente genetista o altra figura sanitaria con la finalità di passare in rassegna alcuni fattori, quale la familiarità per patologie tumorali in termini di quali parenti siano stati affetti da cancro, di quale tipo di cancro si trattasse in ciascun caso e a che età sia stata posta la diagnosi. Qualora dalla valutazione emerga che sussiste un rischio aumentato di portare una variante nociva del gene BRCA1 o del gene BRCA2, il genetista potrà procedere a prescrivere le indagini genetiche appropriate, purché il paziente accetti di sottoporsi a esami genetici.
Qui di seguito sono riportate le raccomandazioni NCCN per l’esame di BRCA1 e BRCA2 [3]:
- Diagnosi di cancro mammario a un'età ≤ 45 anni
- Cancro mammario multiplo: bilaterale o ipsilaterale
- Cancro mammario e ovarico a qualsiasi età
- Cancro mammario nell’uomo
- Cancro mammario triplo-negativo (negativo per recettori per gli estrogeni, negativo per recettori per il progesterone e negativo per HER2/neu) diagnosticato a un'età ≤ 60 anni
- Cancro pancreatico a qualsiasi età
- Due o più parenti (≤ 50 anni di età) con cancro mammario
- Tre o più parenti con cancro mammario a qualsiasi età
- Una mutazione di BRCA1 o BRCA2 identificata in precedenza nella famiglia
- Storia personale di cancro mammario all’età di 46 – 50 anni e un parente stretto con cancro mammario, ovarico, pancreatico o prostatico
- Storia personale di cancro mammario a qualsiasi età e un parente stretto con cancro mammario all’età di 50 anni o più giovane, o due o più parenti stretti con cancro mammario a qualsiasi età
- Cancro prostatico metastatico a qualsiasi età
I soggetti che ereditano tali mutazioni si trovano ad affrontare un rischio elevato di sviluppare cancro mammario nel corso della vita. Una volta posta diagnosi di cancro mammario invasivo, essi presentano un rischio elevato di sviluppare un secondo cancro mammario ipsilaterale o controlaterale[4].
Pertanto, una diagnosi corretta di presenza di tali mutazioni della linea germinale unitamente a idonee strategie di prevenzione screening sono di massima importanza nella lotta a tale malattia.
Tracciante linfatico Magtrace® per l’individuazione di linfonodi sentinella
Molti trattamenti in oncologia implicano una biopsia dei linfonodi sentinella. I linfonodi sentinella sono i primi linfonodi drenanti e, pertanto, presentano il massimo potenziale di ospitare metastasi. La loro rimozione e la loro analisi sono essenziali nel determinare lo stadio del cancro a livello linfonodale, fornendo le indicazioni per un piano di trattamento individuale per il paziente.
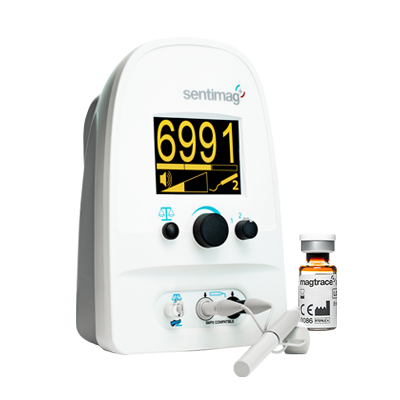
Il tracciante paramagnetico Magtrace® è un tracciante liquido che è stato sviluppato specificamente per la procedura SLNB che viene portata a termine contestualmente alla rimozione del tessuto canceroso sospetto a livello mammario.
Affinché contribuisca all’identificazione dei linfonodi sentinella, il tracciante viene iniettato nella mammella da dove, poi, migrerà attraverso il sistema linfatico sino ai linfonodi sentinella [5]. Grazie a questo segnale tracciabile, per mezzo del sensore magnetico della sonda Sentimag®sarà possibile identificare i linfonodi che contengono Magtrace® prima di rimuoverli, al fine di determinare la diffusione del carcinoma.
Rimozione di lesioni mammarie non rilevabili alla palpazione con Magseed®
Nel momento in cui avviene l’identificazione di un cancro mammario in stadio iniziale o di un nodulo sospetto, la chirurgia conservativa può essere un’opzione - anche nota come nodulectomia o mastectomia parziale.
Si tratta, in tal caso, di una procedura chirurgica che punta a rimuovere completamente la lesione e un margine sottile di tessuto sano intorno alle lesione stessa, facendo sì che non vengano lasciate in sede di lesione cellule tumorali e che si conservi, al contempo, quanto più tessuto sano possibile.
Per localizzare esattamente la lesione durante l’intervento, alcuni adiuvanti sono utilizzati come marcatori – Magseed® è uno di questi marcatori.
Prima dell’intervento chirurgico, il Magseed® viene collocato nel centro della lesione sotto guida radiografica o ecografica. Il posizionamento può essere programmato per una maggiore comodità sia per il paziente che per lo staff ospedaliero. Successivamente, questo minuscolo seme di soli 1 x 5 mm di dimensione resta saldo nella sede in cui è stato posto senza causare disagio per il paziente sino al giorno dell’intervento [6].
Durante l’intervento, la sonda del sistema Sentimag® viene utilizzata per localizzare con precisione Magseed®, e quindi la lesione in cui il Magseed® è posto. Ciò consente di rimuovere il tumore accuratamente e per intero.
Watch the Video with Radiologist Dr Marie-Rose El Bejjani from Hospital Saint-Joseph in Paris and learn more about the placement with Sentimag®-Magseed®.
Watch the Video with breast surgeon Dr Severine Alran from Hospital Saint-Joseph in Paris and learn more about surgery with Sentimag®-Magtrace®.
Dissezione ascellare mirata utilizzando Sentimag®-Magtrace®/Magseed®
In alcuni casi, il piano di trattamento del cancro mammario include una chemioterapia neoadiuvante - una chemioterapia erogata prima dell’intervento. Ciò consente uno stretto monitoraggio della risposta e, secondo studi, il tumore a livello mammario può ridursi e i linfonodi intaccati dal cancro possono virare da “positivi” a “negativi” (privi di cancro) durante il corso della chemioterapia. Aumentano, così, le probabilità di ricevere successivamente un approccio chirurgico meno invasivo, ad esempio una chirurgia di conservazione della mammella.
Qualora siano individuati linfonodi sospetti a livello ascellare al momento della diagnosi, essi sono di norma marcati prima della chemioterapia neoadiuvante o durante la stessa. A questo scopo, un marcatore Magseed® può essere inserito nell’uno o nei linfonodi sospetti, assicurandone un’identificazione e rimozione accurata con l’aiuto del rilevatore Sentimag® durante il successivo intervento chirurgico.
In più, viene anche eseguita una SLNB utilizzando il medesimo strumento, per cui il tracciante liquido Magtrace® viene iniettato nella mammella e migra ai linfonodi sentinella. Il sensore magnetico nella sonda Sentimag® rileverà poi il segnale proveniente dalle particelle di Magtrace® e identificherà i linfonodi associati [7].
La combinazione di queste due procedure è detta dissezione ascellare mirata (TAD). Essa è divenuta di uso più comune, poiché dai primi studi è risultata essere più accurata nel determinare lo stato dell’ascella dopo chemioterapia e nel valutare se il paziente sia sceso di stadio o, nella migliore delle ipotesi, sia pervenuto a uno stato privo di cancro.
Axillary management after neoadjuvant treatment
Sentigmag®-Magseed® / Magtrace® and Osna
Produttore: Sentimag®, Magseed® e Magtrace® sono prodotti da Endomagnetics Ltd (Endomag)
Sentimag® e Magseed® sono marchi commerciali di Endomagnetics Ltd registrati nell’Unione Europea
Magtrace® è un marchio commerciale registrato di Endomagnetics Ltd nel Regno Unito
Valutazione dei linfonodi a livello molecolare con OSNA
Il cancro mammario tipicamente si diffonde per prima cosa ai vicini linfonodi nel cavo ascellare. Durante la chirurgia, i linfonodi sentinella (SLN) sono rimossi e analizzati per rilevare la presenza di metastasi - questa procedura è detta biopsia dei linfonodi sentinella (SLNB).
A seconda dell’entità del carico tumorale presente nei linfonodi SLN, il chirurgo decide se sia o non sia necessaria un’ulteriore dissezione dei linfonodi ascellari. Pertanto, un metodo accurato, affidabile e rapido per l’analisi dei linfonodi SLN è di massima importanza nella gestione del cancro mammario. Un approccio meno invasivo con SLNB consente di risparmiare molte asportazioni a livello ascellare, migliorando la qualità di vita del paziente.
OSNA è un esame diagnostico innovativo su base molecolare per la stadiazione accurata e rapida dei linfonodi in grado di rivelare l’intero quadro linfonodale con sensibilità molto elevata. Il suo valore clinico va al di là della pura valutazione dei linfonodi, poiché esso supporta decisioni di trattamento personalizzate e migliora la qualità di vita del paziente.
Si invita a guardare il video con il dottor Vicente Peg dell’University Hospital Vall d'Hebron, Barcellona, e ad acquisire più informazioni sulla stadiazione intraoperatoria molecolare dei linfonodi con OSNA.
Diagnostica di precisione per la selezione di terapie mirate nel cancro mammario - porta alla luce con precisione quanto deve essere visto
La diagnostica di precisione è la chiave per selezionare la giusta terapia nel giusto momento per il giusto paziente affetto da cancro.
Alterazioni geniche giocano un ruolo cruciale durante l’esordio e lo sviluppo di un cancro mammario. Pertanto, una valutazione affidabile della condizione mutazionale dei tumori è decisiva non soltanto nel selezionare pazienti affetti da cancro eligibili per terapie mirate, ma anche in un secondo tempo nel monitorare la risposta al trattamento e la progressione di malattia.
Attualmente, è disponibile una gamma di medicamenti che mirano ad alterazioni genetiche tumore-specifiche e possono essere prescritti al posto di, o in combinazione con, chemioterapie, immunoterapie e radioterapie standard.
Un’amplificazione di HER2 si osserva in approssimativamente il 15% dei casi di cancro mammario e, in assenza di terapia, si associa a una prognosi infausta [8,9]. Il trattamento di pazienti che presentano un’amplificazione di HER2 con l’anticorpo monoclonale Herceptin® (trastuzumab) si è dimostrato efficace, portando a un incremento della sopravvivenza [10,11].
Inoltre, il gene FGFR1 si è dimostrato amplificato in approssimativamente il 10% di pazienti affetti da cancro mammario. Esso indica un esito infausto, dal momento che una sovraespressione del prodotto genico era implicata in casi di recidive precoci [12-14].
Nel cancro mammario si osserva anche un’amplificazione del gene TOP2A, frequentemente con una co-amplificazione di HER2 [15,16]. Aberrazioni del gene TOP2A costituiscono un marcatore di risposta alla chemioterapia a base di antracicline in pazienti affetti da cancro mammario [12].
Per studiare tali cambiamenti a livello genetico, gli oncologi possono servirsi di vari esami di genetica molecolare a supporto di decisioni di trattamenti personalizzati. Sysmex offre una gamma di prodotti basati su tecnologie di biologia molecolare innovative che supportano professionisti di area sanitaria e pazienti lungo l’intero percorso di cura.
Selezione della terapia
Con le sonde CytoCell® FISH (Fluorescence In Situ Hybridisation) * per i geni HER2 (ERBB2), FGFR1, TOP2A, MET, EGFR e RB1, gli oncologi otterranno specifiche informazioni su geni raggiungibili da farmaci e marcatori prognostici chiave.
Scarica la brochure Sonde per patologia di CytoCell per il cancro mammario
Ulteriori geni implicati nel cancro mammario cruciali e attualmente pertinenti, ivi inclusi BRCA1, BRCA2, TP53 e PIK3CA, possono essere studiati con esami di sequenziamento di nuova generazione con la soluzione Sysmex – SureSeqTM myPanelTM* Pannello su misura per cancro mammario NGS.
Scarica la brochure SureSeq per cancro mammario + pannello CNV
* Sonde FISH di CytoCell®: Ad esclusivo uso del laboratorio. Non inteso per un uso come diagnostica a sé stante o diagnostica di affiancamento. L’azione terapeutica non va avviata sulla base del solo risultato di FISH.
* SureSeqTM myPanelTM: Solo per uso in ambito di ricerca. Non utilizzabile in procedure diagnostiche.
Produttore e nomi commerciali: Sonde FISH di CytoCell® (Cytocell Limited), SureSeqTM myPanelTM (Oxford Gene Technology IP Limited)
Monitoraggio della terapia e delle recidive
Malgrado un trattamento primario chirurgico e/o sistemico, sino al 30% di pazienti affetti da cancro mammario si trova a dover affrontare la progressione di malattia. Così, monitorare i pazienti in termini di risposta alla terapia, in particolar modo in termini di mutazioni di resistenza e ricadute del tumore, è di vitale importanza per garantire il miglior esito a lungo termine possibile per il paziente.
Nell’oncologia moderna personalizzata, talune alterazioni di geni somatici si sono dimostrate biomarcatori chiave per la progressione di malattia, ed esse sono rilevabili nel DNA derivante da tessuto tumorale o nel DNA derivato da tumore circolante (ctDNA) rilevato in una biopsia liquida. Accade spesso che, nello stadio del monitoraggio, campioni di tessuto non siano disponibili per un’analisi. Tuttavia, biopsie liquide possono essere campionate ripetutamente con minimo disagio per il paziente e si sono dimostrate in grado di superare i limiti delle biopsie tissutali, quali perdita di eterogeneità tumorale, minore accessibilità del campione e lunghi tempi di evasione.
L’individuazione di mutazioni clinicamente rilevanti da un semplice prelievo di sangue consente, quindi, agli oncologi di selezionare la terapia di maggiore beneficio e di monitorare la risposta del paziente alla terapia in tempo reale
I kit RUO Plasma-SeqSensei™ (PSS) sono saggi su biopsia liquida basati sul sequenziamento di nuova generazione (NGS), intesi alla ricerca di mutazioni “azionabili” di pertinenza nel cancro colorettale, NSCLC, mammario e della tiroide nonché nel melanoma. Fondata sulla tecnologia SafeSEQ ultrasensibile, la gamma di kit RUO PSS punta a stabilire un nuovo standard per la determinazione assoluta di molecole mutanti (MM) indipendentemente da input di DNA da campione reale, offrendo così ai ricercatori uno strumento innovativo nel promuovere un'oncologia personalizzata. Per via della sua capacità di determinare basse frequenze di alleli varianti, esso è specialmente utile nell’identificare la minima malattia residua (MRD) e per altre applicazioni che richiedano una misurazione in sequenza come monitoraggio di risposta, ricaduta o resistenza.
* Il kit RUO BC Plasma-SeqSensei™ è solo per uso in ambito di ricerca. Non utilizzabile in procedure diagnostiche.
Scopri di più su come Sysmex contribuisce a fare la differenza nella lotta per sconfiggere il cancro al seno
Riferimenti bibliografici
- Sung H. et al. (2021). Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin., 71(3):209-249.
- Paluch-Shimon S. et al. (2016). Prevention and screening in BRCA mutation carriers and other breast/ovarian hereditary cancer syndromes: ESMO Clinical Practice Guidelines. Ann Oncol., 27 (5): v103-v110.
- National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: Genetic/Familial High-Risk Assessment: Breast and Ovarian. V3.
- Kotsopoulos J. (2018). BRCA Mutations and Breast Cancer Prevention. Cancers, 10(12), 524.
- Pedro L. et al. (2019): Impact of locally administered carboxydextran-coated super-paramagnetic iron nanoparticles on cellular immune function. Small, 15, 1900224.
- Kühn F. et al. (2020): A German study comparing standard wire localization with magnetic seed localization of non-palpable breast lesions. In vivo, 34, 1159-64.
- Pohlodek K. et al. (2019): Localization of impalpable breast lesions and detection of sentinel lymph nodes through magnetic methods. Eur. J. Radiol., 120, 108699.
- Tsai-Pflugfelder M, et al. Proc Nat Acad Sci 1988;85:7177-81.
- Bofin AM, et al. Cytopath 2003;14(6):314-9.
- Fountzilas G, et al. BMC Cancer 2013;13:163.
- O’Malley, et al. J Natl Cancer Inst 2009;101(9):644-650.
- Letessier A, et al. BMC Cancer 2006, 6:245.
- Courjal F et al., Cancer Res 1997;57(19):4360-7
- Turner N et al., Cancer Res 2010;70(5):2085-94
- Bofin AM, et al. Cytopath 2003;14(6):314-9.
- Fountzilas G, et al. BMC Cancer 2013;13:163